Scientific journal
Scientific Review. Fundamental and Applied Research
TECHNOLOGY OF OBTAINING AND INVESTIGATION OF PHYSICO-CHEMICAL PROPERTIES OF POLYCOMPHEX COMPOSITES BASED ON NATRICARBOXYMETHYLCELLULOSE
Большую значимость в решении ряда практически важных задач приобретает создание нового класса высокоэффективных материалов, отвечающих современным требованиям научно-технического прогресса. В частности, к ним следует отнести поликомплексы (ПК) и поликомплексные композиты (ПКК), которые обладают уникальными свойствами. Они находят всё более широкое применение в фармации в качестве загустителей, стабилизаторов суспензий, пролонгатора действия лекарственных веществ, пленкообразователя для капсул и таблеток, а также как основы для мягких лекарственных препаратов и др.
Поликомплексы весьма перспективны, занимают важное место в технологии материалов, технике, медицине, других областях народного хозяйства, поскольку обнаруживают ряд уникальных и наиболее ценных свойств. Кроме того, способность многих полиэлектролитов взаимодействовать с другими полимерными соединениями открывают широкие перспективы в области модификации и управляемого синтеза макромолекулярных систем. Благодаря этому из большинства известных веществ, в принципе, можно получить совершенно новые материалы [1, 2].
Весьма интересными, перспективными в этом аспекте являются поликомплексные композиты на основе производных целлюлозы - полианиона натрийкарбоксиметилцеллюлозы (Na-КМЦ), синтетических мочевиноформальдегидных олигомеров (МФО) линейного и циклоцепного строения [3].
Экспериментальная часть.
В работе использовали очищенную натриевую соль карбоксиметилцеллюлозы (Na-КМЦ) продукт Наманганского химического завода, со степенью замещения 70 и степенью полимеризации 450. Второй компонент поликомплекса относится к азотосодержащим полимерам, который получен на основе мочевины и формальдегида. Использовали мочевину марки ч.д.а. без дополнительной очистки, ГОСТ 6691-77, формалин марки "ФМ"-30-40%-ный раствор формальдегида в воде, содержание метанола 5-11%. Реакционные смеси готовили при смешении концентрированных (С=0,4 осн.молъ/л) растворов Na-КМЦ и МФО в определенных технологических условиях и в определенных соотношениях компонентов [4,5].
рН растворов электролитов и их смесей проводили на универсальном иономере ЭВ -74 с использованием стеклянного (измерительный) и хлоросеребристого (сравнительный) электродов. Точность измерения рН – 0,2 ед. рН. Перед измерением прибор настраивали по стандартным растворам. Титрование проводили при постоянном перемешивании и при температуре 22-240С. Определение потери в массе при нагревании образцов проводили согласно методики ГФ XI, вып.I с 114.. 1 г препарата (точная навеска) помещали в предварительно высушенный и взвешенный бюкс с диаметром 35 мм и высотой 60 мм и нагревали на кипящей водяной бане в течении 1 часа. Затем помещали в эксикатор для охлаждения на 50 мин и взвешивали. Исследование реологических свойств концентрированных растворов полимеров и ИПК проводили на ротационном вискозиметре «Реотест-2» в системе коаксиальных цилиндров в интервале напряжений 2-380 и скоростей сдвига от 1,5 до 13µ10см-1 при различных температурах [6].
Возможности практического использования поликомплексов и композиционных материалов в фармации в значительной степени определяется комплексом физико-химических, физико-механических и технологических свойств. На рис.1 представлены изменения технологических параметров поликомплексных композитов в зависимости от соотношения составляющих компонентов Nа-КМЦ и МФО. Из рис.1 видно, что параметры растворимости и вязкости уменьшаются, а показатель рН и потери в массе увеличиваются в зависимости от соотношения компонентов исследуемых веществ.
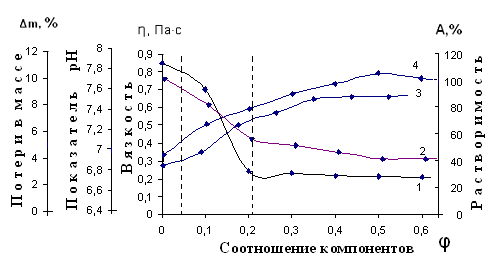
Рис.1. Зависимость вязкости (1–η, Па•с), растворимости (2 – А, %),
показателя рН (3 – pH) и потери в массе (4 – Δm, %) от
соотношения компонентов поликомплексных основ
Nа-КМЦ:МФО
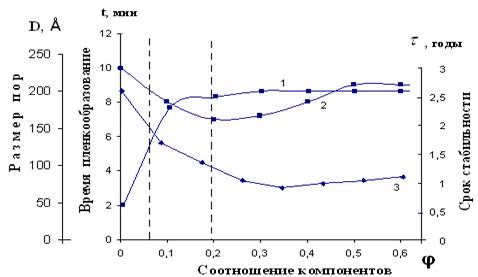
Рис.2. Зависимость срока стабильности (1– 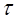 , годы), время
, годы), время
пленкообразования (2 – t, мин) и размера пор (3 – D, Å)
поликомплексных мембран от соотношения Nа-КМЦ-МФО
Следует отметить, что показатель рН, должен быть в области нейтрального значения вещества (рН =5-7). А потери в массе для данных веществ по нормативно-техническим данным не должны превышать 14%. Результаты исследований вышеуказанных параметров показывают пересечение кривых в определенной области соотношении компонентов основ. Аналогичные данные были обнаружены на рисунке 2, в частности, кривая изменения размеров пор в зависимости от соотношения компонентов снижается (рис. 2, кр.3), а кривая срока стабильности возрастает (рис.2, кр.1). Следует отметить, что кривая времени пленкообразования имеет минимум в области пересечения двух вышеуказанных параметров, т.е. срока стабильности и совместимости.
Таким образом, выбор оптимального соотношения компонентов исследуемых объектов соответствует области, заключенной штрих-пунктиром (рис. 1, 2).
Одним из основных свойств поликомплексов и композиционных материалов при применении как основы для мягких лекарственных форм является стабильность при хранении. Под стабильностью понимают их не прогоркаемость при хранении, не изменяемость от действия бактерий, кислорода, влаги, температуры, и не расслаеваемость. Поэтому для выбора оптимальной температуры получения поликомплексов и композиционных материалов как основы для лекарственных препаратов учитывали срок стабильности в зависимости от температуры (рис.3). Из рис.3 видно, что ход кривых зависимостей исследуемых объектов одинаков и срок стабильности уменьшается с повышением температуры. Исходя из этих результатов, была выбрана оптимальная технологическая температура в области 20 – 25ºС.
На основании экспериментальных данных установили, что основа полученная с помощью Nа-КМЦ и МФО легко наносится на кожу и сохраняет свою гомогенность и стабильность при длительном хранении. Также были определены качественные показатели такие, как: цвет, запах, внешний вид, рН, агрегативная стабильность при центрифугировании и при влиянии температуры, а также срок хранения основы, отвечающие всем требованиям нормативно-технической документации.
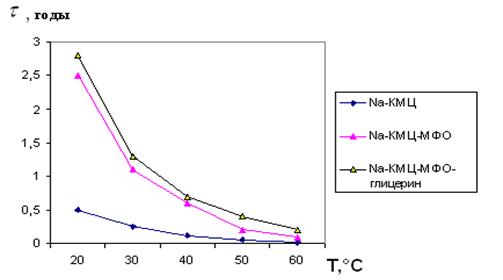
Рис.3. Изменение срока стабильности поликомплексных
основ в зависимости от температуры: 1. Nа-КМЦ, 2. Nа-КМЦ- МФО;
- Nа-КМЦ- МФО – глицерин.
Исходным продуктом для приготовления «ПКГ-1» был выбран натрий–карбоксиметилцеллюлоза – чисто медицинский продукт Наманганского химического завода со степенью замещения 70 и полимеризации 450 - ТУ 6-55–39-90, мочевина-формальдегидный олигомер – ГОСТ 1431- 78, свежеприготовленный без примесей и глицерин – ФС 42 Уз -0035 -2002.
Технологическая схема получения ПКК состоит из одной линии (рис.4). Технологический процесс получения ПКК на основе промышленной Nа-КМЦ и МФО начинается со стадии растворения Nа-КМЦ, далее идет перемешивание раствора Nа-КМЦ с МФО, перемешивание реакционной смеси с глицерином и образование ПКК на базе Nа-КМЦ и МФО.
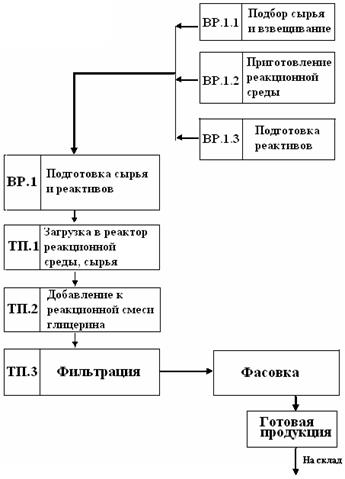
Рис.4. Технологическая схема производства поликомплексных
композитов на основе
Nа-КМЦ и МФО
ВР.1.1, ВР.1.2, ВР.1.3 – вспомогательные работы;
ТП.1, ТП.2, ТП.3 –
технологические процессы.
Растворы поликомплексного композита приготовляются следующим образом (рис.5): в емкость реактора (3) заливают дистиллированную воду (4) до половины отметки. Включается – мешалка реактора. Сухой очищенный компонент Na-КМЦ (1) подается в количестве, предусмотренном технологическим регламентом посредством весового мерника (2) в реактор равномерными порциями с одновременным перемешиванием. Далее воду наполняют до полной отметки. После прибавления всего количества Na-КМЦ смесь перемешивают в течение 4-5 часов до получения однородной массы. При перемешивании в реактор (3) заливают раствор МФО (5) в количестве 10% от общей массы Na–КМЦ. Потом при постоянном перемешивании добавляют глицерин (6) в количестве 20% от общей массы поликомплексного композита. Готовый раствор поликомплексного композита перемешивают до образования однородной массы. После анализа готового поликомплексного композита его пропускают с помощью вакуумного насоса (7) через фильтр (8) и расфасовывают с помощью фасовочной машины (9) в полиэтиленовые флаконы.
Реакция формирования комплекса и образования ПКК на основе Nа-КМЦ-МФО происходит гомогенно в водной среде с равномерным начальным распределением сольватированных макромолекул Nа-КМЦ и молекулярно агрегированных Nа-КМЦ в водной среде, далее при добавлении водных систем МФО в реакционную среду, происходит формирование ПКК, с равномерным распределением гелевых форм Nа- КМЦ-МФО ПКК в водной системе, поэтому получение и перемешивание ПКК в реакционной смеси проводится непосредственно в реакционном аппарате – реакторе. При этом модуль реакции, т.е. соотношение Nа-КМЦ:МФО должно быть не ниже 10:1.
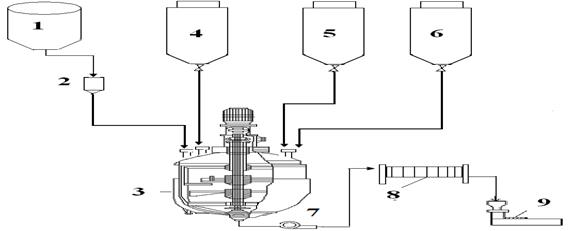
Рис. 5. Аппаратурная схема производства ПКК на базе Nа-КМЦ и МФО:
1- сухой компонент натрийкарбоксиметилцеллюлозы; 2 – весовой мерник; 3 – реактор;
4 – растворитель; 5- раствор мочевиноформальдегидного олигомера; 6 – глицерин;
7- вакуумный насос; 8 – фильтр; 9 – расфасовочная установка.
Таким образом, разработана технология получения поликомплексных композитов на базе натрийкарбоксиметилцеллюлозы с мочевиноформальдегидными олигомерами как основы для мягких лекарственных препаратов пролонгированного действия с оптимальными физико-химическими, физико-механическими и эксплуатационными характеристиками. Установлена возможности использования поликомплексных композитов на основе Na-КМЦ-МФО в качестве основы для лекарственных систем с направленными транспортными свойствами и контролируемым выделением лекарственных препаратов.
Выводы:
- Впервые предложен новый гелевой поликомплексный композит на основе Nа-КМЦ–МФО, в которой, благодаря оптимальному сочетанию компонентов, регулируемому молекулярному строению полимерного комплекса в результате самоорганизации макромолекул в процессе его формирования, образуются структуры с регулируемыми размерами.
- Разработана технология получения поликомплексных композитов на базе натрийкарбоксиметилцеллюлозы с мочевиноформальдегидными олигомерами как основы для мягких лекарственных препаратов пролонгированного действия с оптимальными физико-химическими, физико-механическими и эксплуатационными характеристиками. Составлена технологическая схема производства поликомплексных композитов и установлены основные технологические параметры в производственных условиях.
- Показана возможности использования гелей ПКК на основе Na-КМЦ-МФО в качестве основы для лекарственных систем с направленными транспортными свойствами и контролируемым выделением лекарственных препаратов.
Библиографическая ссылка
Инагамов С.Я., Ходжаев Ф.М., Муратов С.С. ТЕХНОЛОГИЯ ПОЛУЧЕНИЯ И ИССЛЕДОВАНИЕ ФИЗИКО-ХИМИЧЕСКИХ СВОЙСТВ ПОЛИКОМПЛЕКСНЫХ КОМПОЗИТОВ НА ОСНОВЕ НАТРИЙКАРБОКСИМЕТИЛЦЕЛЛЮЛОЗЫ // Научное обозрение. Фундаментальные и прикладные исследования. 2018. № 1. ;URL: https://scientificreview.ru/en/article/view?id=15 (дата обращения: 03.05.2026).
